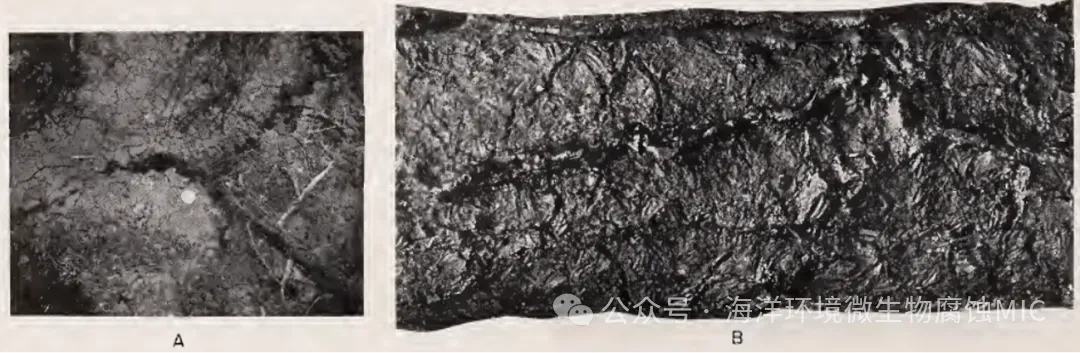
1910 年,Gaines报告了对厌氧腐蚀的铁结构中富硫腐蚀产物的分析结果,并推测其与细菌硫循环存在关联(Bacterial Activity as a Corrosive Influence in the Soil.)。高硫化物的腐蚀锈层存在于高有机质含量的服役环境下。模拟电化学腐蚀环境验证出硫含量生成量减少,并且输水管道天然硫的含量很低,锰含量较低的情况下结合硫含量更少。考虑到铁与氧结合的倾向性极强,则与硫的结合性也应该被考虑。
2. von Wolzogen Kühr CAH, vander Vlugt LS. 1934. The graphitization of cast iron as an electro-biochemical process in anaerobic soil. Water18:147–165.
1934 年von Wolzogen Kühr和van der Vlugt的研究确定 SRB 是北荷兰富含硫酸盐土壤中广泛出现的铁管故障的主要原因。作者提出了一种纯粹的无机营养微生物过程,其中铁是唯一的还原当量。他们将微生物腐蚀归因于一种显著的生理特性,即 SRB 将阴极氢作为唯一的电子供体。这种机制解释后来以经典“阴极去极化理论”而闻名。
土壤中的铸铁腐蚀是微生物腐蚀研究历史中的重要部分。早在20世纪30年代,荷兰人库尔和维卢特(1934)和英国人邦克(1939)就提到微生物对铁和钢的厌氧腐蚀问题。赫德莱(1940)特别指出,在渍水沼泽地中的金属腐蚀与微生物活动密切相关,他提出细菌腐蚀试验可以进行细菌分析,并把腐蚀盐类做硫化物分析。
对土壤中铸铁腐蚀的研究开启了微生物腐蚀研究的历史。通过对这一现象的观察和分析,逐渐认识到微生物在金属腐蚀过程中所起的作用。Underground Corrosion列出了一系列与地下腐蚀相关的早期研究成果,涵盖了从1923年到1957年期间的研究,内容涉及微生物厌氧腐蚀、土壤中硫化物对铁腐蚀的影响、铁和钢的细菌腐蚀等多个方面,为理解地下腐蚀的理论和实践提供了重要的参考依据。
K. H. Logan, Underground Corrosion, DP - 1936, Transactions of the American Society of CivilEngineers, 811-825, 101, 10.1061/TACEAT.0004751.
3. Costello.1974. The mechanism of cathodic depolarization exhibited by sulphate-reducing bacteria during metallic corrosion processes. S. Afr. J. Sci. 70, 202-204.
20 世纪 60 年代初,研究发现细菌培养物消耗阴极氢的能力与铁腐蚀中阴极反应的刺激“去极化”之间似乎存在关联。尽管von Wolzogen Kühr和van der Vlugt最初提出的基于无机营养的概念,但后来的许多实验都使用乳酸盐作为额外的有机电子供体来进行硫酸盐还原。Costello指出,在“无有机碳”饥饿状态下,SRB 仍可使阴极电流显著增大,钢材失重腐蚀速率可达 0.7 mm y⁻¹。若按 CDP 理论,SRB 应把阴极产生的 H₂ 迅速消耗掉,从而降低阴极过电位、加速腐蚀。但 Costello 测得体系内并未出现明显的“氢消耗”证据,阴极去极化现象仍可发生。因此认为真正具有去极化作用的并不是细菌对 H2的清除,而是细菌代谢生成的硫化氢(H2S)以及随后与 Fe2+形成的导电 FeS 膜。这层膜本身可作为高效阴极,扩大有效阴极面积,形成“硫化物-钢铁”电偶对,从而加速阳极溶解。
SRB 的腐蚀性似乎完全可归因于它们产生的硫化氢。硫化氢是一种高反应活性的阴极和阳极反应物。硫化氢会迅速与金属铁发生反应[净反应:H₂S + Fe⁰ → FeS + H₂,ΔG° = - 72.5 kJ/(mol Fe0)],从而形成特征性的腐蚀产物硫化铁。20 世纪 60 年代末至 70 年代初,几位作者证明,这种生物成因的硫化铁沉积在金属上时会加速腐蚀。有趣的是,硫化铁持续引发的腐蚀需要有活跃的 SRB 种群存在。在这种腐蚀情形中的确切机制尚未完全明确。
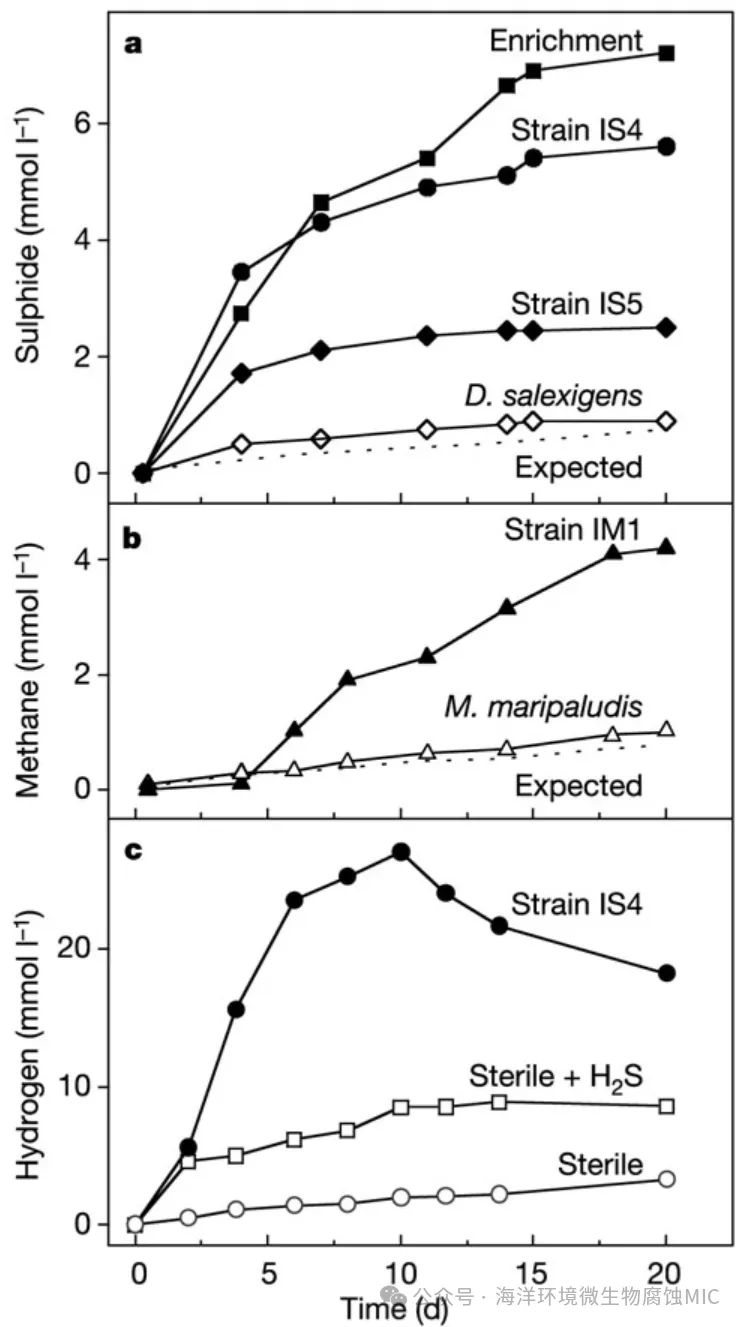
4. Dinh, H., Kuever, J., Mußmann, M. et al. Iron corrosion by novel anaerobic microorganisms. Nature 427, 829–832 (2004). https://doi.org/10.1038/nature02321.
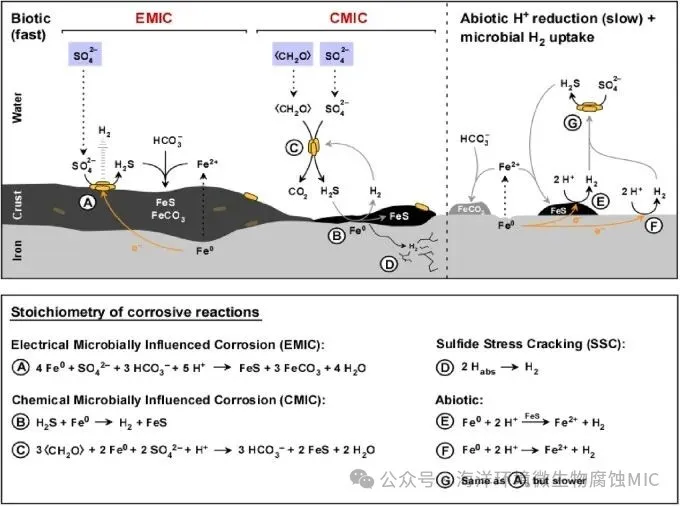
2004 年,通过从以金属铁作为唯一电子供体的海洋沉积物富集培养物中分离出 SRB,为一种新的腐蚀机制提供了实验证据。分离出的IS4菌株进行的硫酸盐还原可能直接由细菌消耗铁源电子提供动力。事实上,在无有机质培养物中培养时,即使是最有效的利用氢气的 SRB 与无菌对照试验相比,也不会加速铁的腐蚀,而这些新分离出的菌株在相同条件下可使铁的氧化速度提高达 71 倍。此前,一些研究人员曾考虑过这种直接摄取电子机制的存在,但当时没有明确的模式生物用于实验验证。Widdel提出了 “电微生物影响腐蚀”(EMIC)这一术语。EMIC 与生物成因 H₂S 的腐蚀效应有着本质区别,它能以具有重要技术意义的速率破坏金属结构。
虽然到目前为止,仅在数量有限的高腐蚀性 SRB 分离物中观察到了 EMIC,但从定义上讲,如果存在硫酸盐和合适的电子供体,所有 SRB 都能通过排泄化学物质 H₂S 来影响腐蚀(即 “化学微生物影响腐蚀”,CMIC)。综上所述,SRB 可作为厌氧铁腐蚀的直接或间接催化剂(分别对应 EMIC 和 CMIC),并且在这方面存在物种特异性差异。
Enning D, Garrelfs J. Corrosion of iron by sulfate-reducing bacteria: new views of an old problem. Appl Environ Microbiol. 2014 Feb;80(4):1226-36. doi: 10.1128/AEM.02848-13.
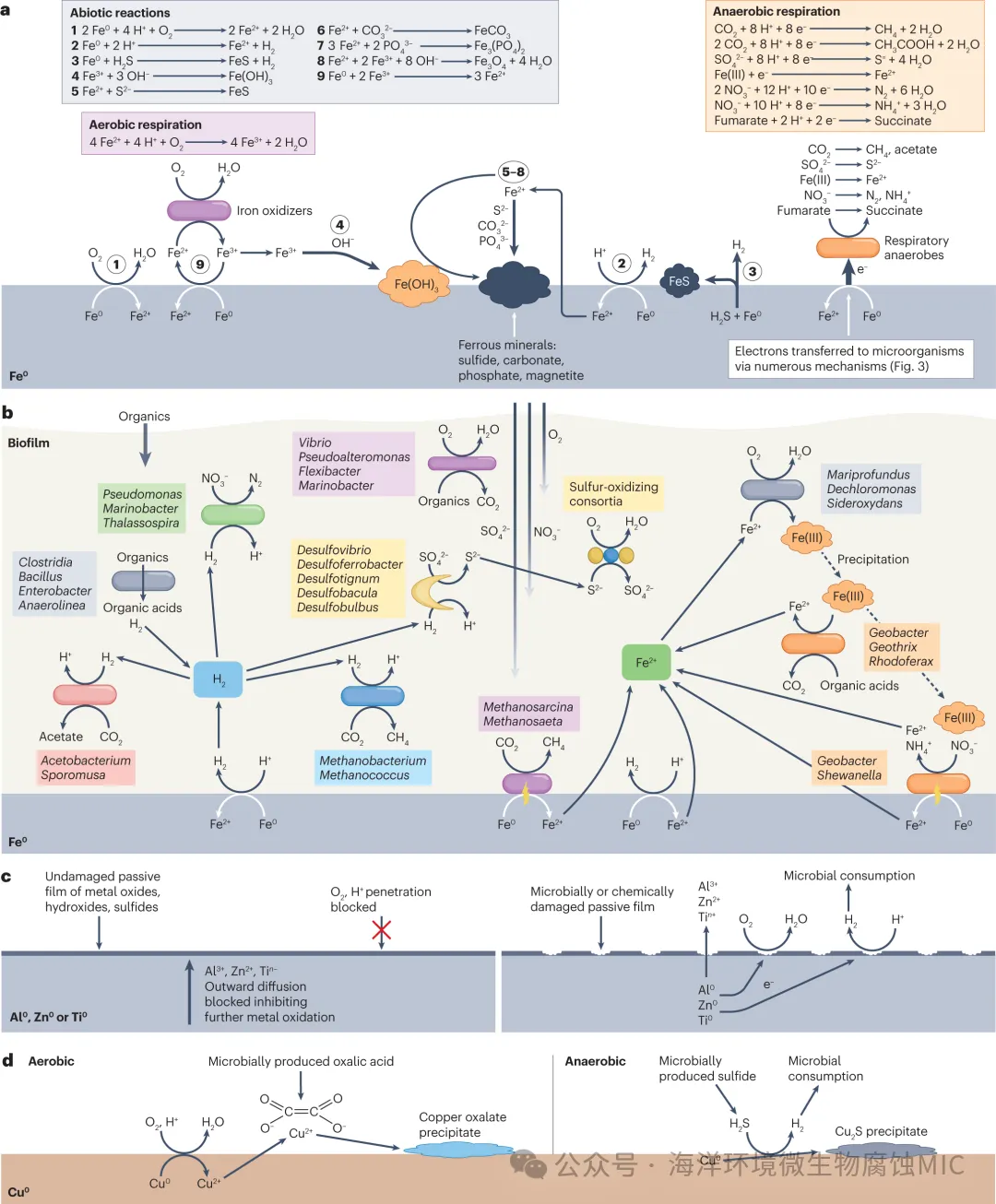
百年的微生物腐蚀研究随着新的表征技术手段的发展而迎来新的动向。各种各样的微生物,通常以生物膜的形式生长,与腐蚀有关。好氧微生物建立了促进金属腐蚀的条件,但大多数腐蚀被归因于厌氧菌。微生物产生的有机酸、硫化物和细胞外氢化酶可以加速金属铁(Fe0)的氧化,从而产生氢气(H2),呼吸厌氧菌也可以消耗H2作为电子供体。一些细菌和古菌直接接受Fe0的电子来支持厌氧呼吸,通常与c型细胞色素作为与金属的明显外表面电接触。功能遗传学研究开始更严格地定义腐蚀机制。组学研究揭示了哪些微生物与腐蚀有关,但需要新的策略来回收培养中的腐蚀性微生物,以评估腐蚀能力和机制。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。

官方微信
《腐蚀与防护网电子期刊》征订启事
- 投稿联系:编辑部
- 电话:010-62316606
- 邮箱:fsfhzy666@163.com
- 腐蚀与防护网官方QQ群:140808415